Istilah Atom pertama kali diperkenalkan oleh Democritus yang diambil dari kata Atomos dalam bahasa Yunani berarti gak dan tomos berarti dibagi.
Dengan kata lain, atom merupakan partikel terkecil yang gak bisa dibagi lagi. Diameternya bisa sekitar 3 sampai 5 nm.
Buat lebih jelasnya lagi, langsung aja yuk ke pembahasan lengkap yang ada dibawah ini.
Pengertian Atom
Atom yaitu partikel paling kecil yang memiliki sifat unsur. Jari-jari suatu atom sekitar 3 – 15 nm (1 nm = 10-9 meter).
Saat ini atom udah bisa dilihat pakai mikroskop STM (Scanning Tunneling Microscope) dan AFM (Atomic Force Microscope), jadi sifat dan karakteristik dari bentuk atom bisa diamati dengan lebih jelas.
Gejala yang ditimbulkan atom bisa kamu pelajari seperti warna nyala, difraksi, sifat listrik, sifat magnet dan gejala lainnya.
Sejarah Penemuan Atom

Teori atom pertama kali dikemukakan oleh John Dalton pada tahun 1803 yaitu atom partikel terkecil yang gak bisa dibagi lagi.
Tapi, kemudian ternyata atom terdiri dari partikel – partikel yang lebih kecil lagi yaitu proton, elektron, dan neutron. Partikel pembentuk atom ini disebut dengan partikel sub atom.
Model atom terus berkembang mulai dari model atom Dalton, Thomson, Rutherford, Bohr sampai model atom modern yang kamu pakai sekarang.
Partikel Penyusun Atom

Partikel dasar pembentuk atau penyusun atom terdiri atas proton, neutron dan elektron. Nah, berikut dibawah ini penjelasannya.
1. Proton
Pada tahun 1886, seorang yang bernama Eugen Goldstein melakukan percobaan memodifikasi tabung sinar katode yang ditemukan William Crookes caranya melobangi lempeng katode.
Dari percobaan ini, menemukan kalo gas yang ada di belakang katode jadi berpijar. Berarti radiasi dari anode menembus lempengan katode lewat lubang yang udah dibuat.
Dibawah ini, ada beberapa hasil percobaan yang dilakukan:
- Sifat sinar anode ini yaitu radiasi partikel karena mampu memutar baling – baling.
- Radiasi ini kalo dibelokkan pakai medan magnet, maka akan menuju ke kutub magnet negatif. Artinya, radiasi sinar ini bermuatan positif (itu penyebabnya yang dinamakan anode dan kemudian dinamakan proton).
- Partikel sinar anode bergantung pada jenis gas yang ada di dalam tabung.
Massa proton terkecil diperoleh pada atom Hidrogen yaitu Massa 1 proton = 1 sma = 1,66 × 10-24 gram dengan muatan 1 proton = +1 = 1,6 × 10-19 C.
2. Elektron
Kemudian, pada tahun 1897 Joseph John Thomson melakukan percobaan pakai tabung sinar katode.
Ada 2 plat elektroda, dimana salah satu plat logam yang ada pada ujung tabung yang berfungsi sebagai katoda.
2 plat ini dimasukkan ke dalam tabung kaca bertekanan rendah, dan dialirkan listrik bertegangan tinggi sampai mampu melepas elektron dari katoda ke anoda.
Sinar katoda gak bisa kamu lihat pakai mata telanjang, tapi kamu bisa mengetahui kalo sinar ini ada dari berpenjarnya lapisan tabung kaca bagian dalam akibat adanya benturan antara elektron dengan dinding tabung.
Kamu bisa melihatnya kalo sinar katoda, coba kamu benturkan ke layar berfluoresensi (layar yang bisa berpendar) setelah kamu beri lubang pada plat logam anoda. Seperti gambar di bawah ini.
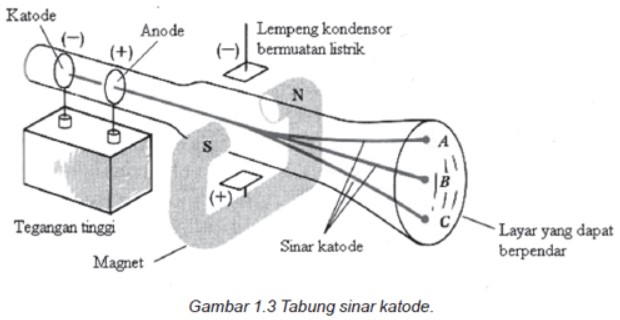
Nah, dibawah ini adalah beberapa hasil percobaan yang dilakukan:
- Merupakan radiasi partikel, karena mampu memutar baling – baling.
- Radiasi ini kalo dibelokkan pakai medan magnet, maka akan menuju ke kutub magnet positif. Artinya, sinar katode bermuatan negatif.
- Partikel katoda merambat tegak lurus dari lempengan katode menuju anode.
- Sinar katoda gak tergantung pada jenis plat logam yang dipakai.
- Sinar katoda bisa kamu buat dengan listrik tegangan tinggi.
Dengan sifat ini, maka J.J Thomson menamakan partikel penyusun atom bermuatan negatif ini sebagai Elektron.
J.J Thomson juga menemukan perbandingan muatan elektron terhadap massa yaitu 1,76 × 108 C/g.
Pada tahun 1909, Robert Millikan berhasil menemukan besarnya muatan sebuah elektron yaitu 1,6 × 10-19 C. Maka kamu peroleh massa 1 elektron sebesar 9,1095×10-31 Kg.
3. Inti Atom
Setelah menemukan proton dan elektron, Ernest Rutherford melakukan penelitian penembakan lempeng tipis.
Kalo atom terdiri dari partikel yang bermuatan positif dan negatif, maka sinar alpha yang ditembakkan harusnya gak ada yang diteruskan/menembus lempeng yang jadi muncul istilah inti atom.
Ditahun 1911, Ernest Rutherford dibantu oleh Hans geiger dan Ernest Marsden, menemukan konsep inti atom didukung oleh penemuan sinar X oleh Wc. Rontgen ditahun 1895 dan penemuan zat Radioaktif pada tahun 1896.
4. Neutron
Pada tahun 1930, prediksi Rutherford mamacu seseorang yang bernama W. Bothe dan H. Becker melakukan eksperimen penembakan partikel alpha pada inti atom berilium Be, ternyata dihasilkan radiasi partikel berdaya tembus tinggi.
Kemudian, ditahun 1932 eksperimen ini dilanjutkan oleh James Chadwick, ternyata partikel yang menimbulkan radiasi berdaya tembus tinggi itu bersifat netral atau gak bermuatan.
Dan massanya hampir sama dengan proton, partikel ini disebut dengan Neutron dan dilambangkan dengan.
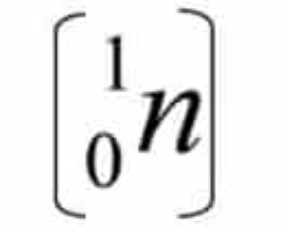
Nah, itulah tadi beberapa pembahasan tentang partikel penyusun atom yang harus kamu ketahui.

